Hoy me encontraba preparando la solución nutritiva concentrada para las plantas y pensando en un tema interesante sobre el cual publicar en el blog y me pareció interesante hablarles un poco sobre los quelatos.
Como ustedes saben, cuando una sal se pone en contacto con agua, el agua la rompe en sus contituyentes iónicos (el agua de hecho forma esferas de hidratación alrededor de dichos iones, los «enlaza» por así decirlo para compensar la energía necesaria para romper el cristal». Por ejemplo, la sal de cocina NaCl, se separa en iones sodio (cargados positivamente) y iones cloruro (cargados negativamente). Estos iones son especies características en solución, es decir, si una planta necesita sodio, busca al cation sodio (la especie cargada positivamente) en solución. Si necesita hierro, busca al hierro y así sucesivamente. Ahí es donde viene el problema.
Si tenemos una cantidad muy grande de iones en solución (una planta necesita, por ejemplo 0.1mg por litro de molibdeno como molibdato, 1mg por litro ya sería una cantidad excesiva), la planta empieza a sufrir y a manifestar las condiciones de toxicidad (exceso) del nutriente. Entonces el truco está en que existan muchos iones que contengan al que la planta necesita, sin ser los que la planta necesita :).
Por ejemplo, tenemos el hierro en solución como ion ferrico (tres cargas positivas), pero tenemos una cantidad monstruosa de él. Entonces añadimos un agente quelante, como el EDTA (ácido etilendiamin tetraacético) en solución y este atrapa al hierro, como en una jaulita y no lo deja salir. La planta no ve hierro sino que ve el quelato (el hierro atrapado por la otra molécula) y ese no le es útil y por lo tanto no lo recoge. Sin embargo el quelato no lo acompleja todo sino que deja cierta cantidad de iones en solución que la planta usa y a medida que los va usando, el equilibrio hace que se vaya liberando el quelato (los iones se van saliendo de su prisión para equilibrar los que la planta toma). Y ahí se tiene, la maravilla de los quelatos.
Lo bueno, es que existen muchos agentes quelantes, para todos los metales de la tabla periódica. Otra ventaja es que al ser lenta la liberación, el impacto ambiental por toxicidad de metales en el suelo es mucho menor y los quelantes (que son moléculas orgánicas) se degradan en el suelo facilmente. De hace un tiempo para acá, me di cuenta que para preparar mi solución concentrada de nutrientes era muy útil el uso del quelato que forman el ión citrato y el ión calcio (que es un quelato que se usa en los suplementos de calcio para humanos también, y se prepara muy facilmente). A los tomates cherry parece gustarles mucho esta formulación. (abajo ven una imagen un quelato, el atomo de calcio se encuentra envuelto por una molécula de EDTA).
–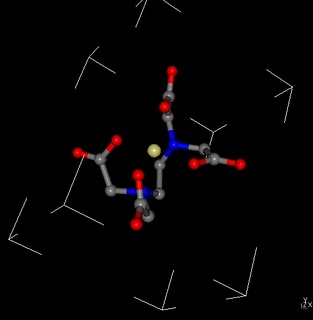 –
–
También, recibí un mail hace poco preguntandome por los costos de los insumos y la constitución de mi solución hidropónica. Dejo entonces un pequeño resumen que espero pueda serles útil. (cantidades por litro de solución concentrada, debe diluirse 100 veces para el riego, precios en pesos colombianos por kilo)
Nitrato de Calcio 4000$/kg 30g
Nitrato de Potasio 2500$/kg 75g
Fosfato de Sodio 10000$/kg 15g
Citrato de Calcio (lo preparo con ácido cítrico 4500$/kg y carbonato de calcio 500$/kg) 5g
Ácido Cítrico 4500$/kg 5g
Para los nutrientes menores, prefiero comprarlos preparados 25000$kg que alcanzan para 20 preparaciones. (se usan 50g)
4 respuestas a “Quelatos en el cultivo y algunos costos”
Estimado Daniel, también soy estudiante de la Universidad Nacional de Colombia (pero de Ingeniería Química) en este momento me encuentro estudiando algunos fertilizantes y me gustaria que me dijera en donde puedo encontrar informacion acerca de la elaboracion de quelatos líquidos y sobre problemas de comaptibilidad entre sales (fosfatos,sulfatos,etc)
Agradezco de antemano su colaboración.
Si desea puede contactarme en el correo andresaltamar@gmail.com
Sr Daniel.
he leeido con interes su nota sobre los quelatos.
Nosotros actualmente usamos el quelato de cobre para tratamiento de agus residuales y despues de 45 dias lo decantamos y le damos un segundo uso para riego y nos da un buen resultado.
De acuerdo a su experiencia como trabaja este quelato en la desintegracion de las aguas negras y porque ayuda a las plantas?
Disculpe mi ignorancia pero mi trabajo es en tratamiento de aguas residuales, y me gustaria saber como trabaja el quelato en el cultivo y si contaminan los residuoas del quelato.
cool!very creative!avdvd,色情遊戲,情色貼圖,女優,偷拍,情色視訊,愛情小說,85cc成人片,成人貼圖站,成人論壇,080聊天室,080苗栗人聊天室,免費a片,視訊美女,視訊做愛,免費視訊,伊莉討論區,sogo論壇,台灣論壇,plus論壇,維克斯論壇,情色論壇,性感影片,正妹,走光,色遊戲,情色自拍,kk俱樂部,好玩遊戲,免費遊戲,貼圖區,好玩遊戲區,中部人聊天室,情色視訊聊天室,聊天室ut,成人遊戲,免費成人影片,成人光碟,情色遊戲,情色a片,情色網,性愛自拍,美女寫真,亂倫,戀愛ING,免費視訊聊天,視訊聊天,成人短片,美女交友,美女遊戲,18禁,三級片,自拍,後宮電影院,85cc,免費影片,線上遊戲,色情遊戲,情色
Hola Daniel,
He descubierto tu blog porque estoy haciendo un proyecto para la universidad sobre un invernadero hidroponico. Mi proyecto de fin de carrera se va a basar precisamente en montar uno, pero no sé exactamente qué materiales necesito para ello. Se tiene que tratar de un invernadero no para autoconsumo sino para producción industrial.
Si pudieras ayudarme sobre qué materiales necesitaría (un invernadero, un sistema de riego, placas,….) te lo agradecería.
Mi email es larrinaga.ander@gmail.com
Muchas gracias de antemano :)